 Milano 15/04/2021. Pubblicato su Cell Reports il lavoro che identifica alcuni regolatori della identità delle cellule beta pancreatiche nell’uomo, frutto della collaborazione dell’ University of Birmingham, del Centro de Investigación Biomédica en red Diabetes y Enfermedades Metabólicas Asociadas (CIBERDEM) di Barcelona, dell’University of Exeter, del Max-Planck Institute for Immunobiology and Epigenetics di Friburgo, dell’ Imperial College di Londra, dell’ INSERM di Parigi e del Diabetes Research Institute di Milano.
Milano 15/04/2021. Pubblicato su Cell Reports il lavoro che identifica alcuni regolatori della identità delle cellule beta pancreatiche nell’uomo, frutto della collaborazione dell’ University of Birmingham, del Centro de Investigación Biomédica en red Diabetes y Enfermedades Metabólicas Asociadas (CIBERDEM) di Barcelona, dell’University of Exeter, del Max-Planck Institute for Immunobiology and Epigenetics di Friburgo, dell’ Imperial College di Londra, dell’ INSERM di Parigi e del Diabetes Research Institute di Milano.
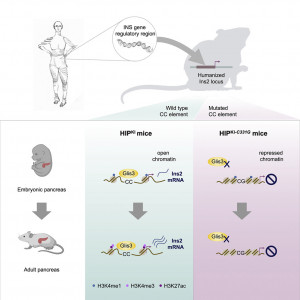
E’ sempre più chiaro che la perdita di identità delle cellule che producono l’insulina sia tra i meccanismi alla base dello sviluppo del diabete. Infatti, le cellule beta pancreatiche per essere efficienti e funzionali devono essere non solo presenti nel pancreas in numero adeguato ma anche raggiungere un grado di maturità che permetta loro di regolare il metabolismo in modo corretto. Questa maturità è mantenuta grazie all’espressione coordinata di una serie di geni, espressione che è orchestrata da un complesso sistema di controllo che necessita lo scambio di informazioni e la loro decifrazione all’interno del DNA. Alcune forme di diabete sono legate a mutazioni dei geni coinvolti nell’identità delle cellule beta, e queste sono più facilmente riconoscibili e studiabili. Le mutazioni però possono riguardare i regolatori. Ogni gene è preceduto da regioni che regolano la sua espressione e su cui dei regolatori denominati fattori di trascrizione agiscono per far esprimere o reprimere il gene stesso. Lo studio e la comprensione del significato delle varianti presenti in queste regioni indirettamente coinvolte è molto più difficile. Uno dei problemi è che il loro studio in vitro non riesce sempre a ricostruire in modo corretto la complessità del sistema e questo limita la nostra comprensione di quali siano le varianti che causano malattia. Per questo motivo si è studiato in 60 soggetti una forma di diabete neonatale recessivo causato da una mutazione della regione (promoter) che controlla l’espressione del gene dell’insulina. Lo studio ha evidenziato che tutte le mutazioni avevano in comune la modifica di un punto preciso del promotore e, per comprenderne il significato, la mutazione è stata modellata umanizzando con l’ingegneria genetica la regione corrispondente del gene dell’insulina nel modello animale. Questo ha permesso di avere un modello adeguato per ricapitolare la complessità evidenziando che la modifica di quel punto impediva l’espressione del gene dell’insulina durante lo sviluppo del pancreas ma soprattutto che quella regione era importante per la funzione di un regolatore (fattore di trascrizione) denominato GLIS3, il cui difetto è anche esso associato allo sviluppo di diabete neonatale. Il risultato quindi è stato quello di riuscire a collegare due difetti genetici umani in un unico meccanismo essenziale (responsabile dell’attivazione dello sviluppo del gene dell’insulina) alla base dello sviluppo del diabete neonatale nell’uomo. “Non è semplice spiegare in poche parole quanto è stato fatto – spiega Lorenzo Piemonti direttore del DRI e uno degli autori del lavoro – Immaginiamo di essere in un condominio con molti appartamenti dove improvvisamente compare una macchia di umidità su un muro. Risalire alla causa non è per niente facile. La prima cosa che si fa è cercare la perdita nel tubo più vicino, ma il più delle volte senza successo. Di conseguenza si cerca più o meno alla cieca la perdita negli appartamenti vicini sperando di trovare il punto di origine del problema. In questo lavoro l’approccio è stato diverso. Si è fatto un modello del condominio in scala ridotta con la ricostruzione esatta dell’impianto idraulico. Si sono simulate le possibili perdite e si è visto quali potevano dare la macchia di umidità, identificando quella più probabile. Quindi si è ritornati nel condominio si è suonato il campanello all’appartamento del 12 piano e rompendo il muro tra la camera da letto e il bagno si è visto che la perdita era proprio lì come suggerito dal modello. Non siamo ancora in grado di riparare la perdita ma sapere dove sono è un ottimo inizio per qualsiasi aspirante idraulico si cimenti nell’impresa ”.
Il Diabetes Research Institute dell’Ospedale San Raffaele di Milano coglie l’occasione per ringraziare tutti coloro che danno fiducia alla nostra ricerca sostenendola con iniziative di supporto e donazioni. Se vuoi sostenerci puoi farlo direttamente cliccando qui.

