 Lago Maggiore, Baveno
Lago Maggiore, Baveno
Un retreat, che letteralmente significa “ritiro”, in ambito di ricerca scientifica diventa un ritiro nel senso davvero quasi spirituale del termine: un retreat scientifico, infatti, è in generale un’occasione unica in cui la ricerca clinica e la ricerca di base si incontrano non solo per conoscersi e comprendersi, ma per trarre l’uno dall’altro nuovi stimoli o idee.
Nelle giornate del 16-17-18 marzo 2018 a Baveno, nei pressi del Lago Maggiore, si è svolto l’appuntamento annuale tra i più importanti dell’ IRCCS Ospedale San Raffaele, ovvero il San Raffaele Scientific Retreat.
Neutrofili e coinvolgimento dell’esocrino nella patogenesi del diabete di tipo 1.
In occasione del Retreat di quest’anno, tra tutti i progetti del nostro istituto di ricerca, quello del gruppo della dott.ssa Manuela Battaglia – che si occupa di studiare il ruolo dei neutrofili nella patogenesi del diabete di tipo 1 – è stato scelto per essere presentato oralmente dalla dott.ssa Federica Vecchio.
Nella presentazione è stata evidenziata la difficoltà che esiste nello studio del diabete di tipo 1 nell’uomo per il mancato accesso a campioni di sangue e sezioni pancreatiche. Il gruppo della dott.ssa Battaglia ha potuto parzialmente superare questo problema grazie a collaborazioni internazionali e alla presenza del centro Trialnet che permette la raccolta di campioni di sangue da parenti di persone diabetiche, classificati come “soggetti a rischio” che costituiscono quindi un elemento indispensabile per gli studi di ricerca mirati a predire il diabete di tipo 1. Sulla base dei dati ottenuti dallo studio, i neutrofili, cellule con una doppia faccia (brave a riparare ma anche a fare danno) e già note per il loro ruolo chiave in altre patologie autoimmuni, sembrano avere un’importante funzione nella prima fase di sviluppo del diabete di tipo 1.
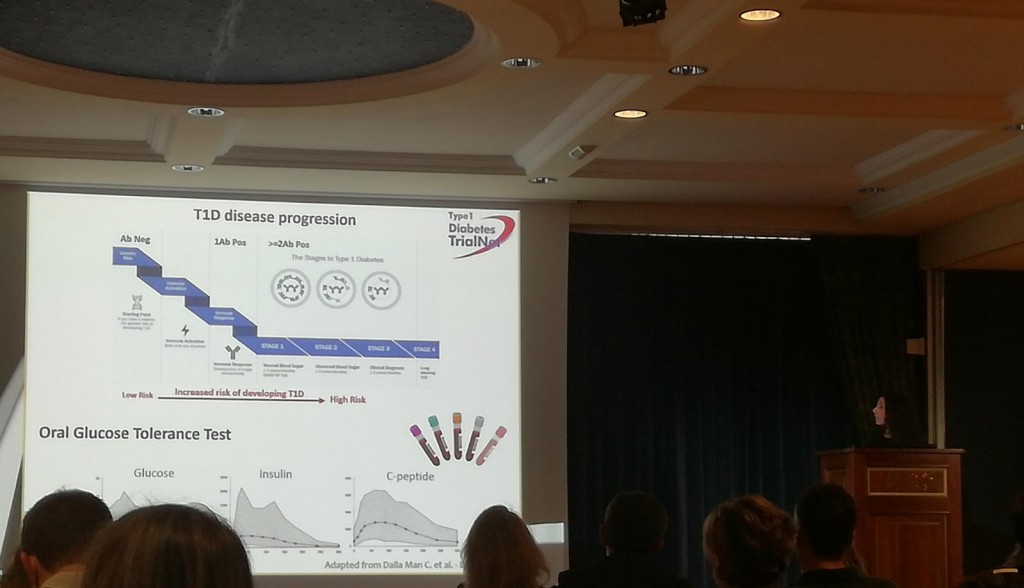 Momenti del Retreat
Momenti del Retreat
Il gruppo della dott.ssa Battaglia si è chiesto anche se il diabete di tipo 1 può essere considerata una malattia dell’intero pancreas.
Il gruppo, in collaborazione con il gruppo del dr. Rampolli – che si occupa di genetica e biologia cellulare – , ha come obiettivo quelli di generare dati che supportino la nuova ipotesi che il T1D sia un disturbo infiammatorio dell’intero pancreas. Al Retreat, la dott.ssa Mandelli, ricercatrice del gruppo Battaglia, ha presentato un poster scientifico in cui si è ipotizzato che il diabete di tipo 1 inizi come una malattia del pancreas esocrino – porzione composta da gruppi di cellule ricche di granuli, all’interno dei quali vengono sintetizzati gli enzimi digestivi.
L’obiettivo finale del progetto è quello di testare se granuli nel pancreas esocrino abbiano un ruolo nel processo infiammatorio che, secondo gli studi, si verifica nelle fasi iniziali della patogenesi del T1D.
Trapianto beta cellulare: come fare quando la memoria immunologica non si scorda del diabete?
Tra i gli altri studi presentati dal nostro istituto di ricerca, ci sono stati inoltre i poster scientifici della dott.ssa Carlotta Bordignon e della dott.ssa Adriana Canu, ricercatrici del gruppo del dr. Paolo Monti, che studia gli aspetti immunologici legati al trapianto di massa beta cellulare.
Nel primo studio presentato, è stato dimostrato che la memoria immunologica dell’organismo non si scorda del diabete ( “Detection and characterization of CD8+ autoreactive memory stem T cells in patients with type 1 diabetes”).
E’ stata infatti evidenziata l’esistenza di cellule staminali della memoria – responsabili del mantenimento della memoria immunologica a lungo termine – capaci di riconoscere gli antigeni delle beta cellule: sostanzialmente, il sistema immunitario è in grado di “ricordare” il primo incontro con un agente patogeno e di reagire in modo pronto e tempestivo ad un successivo incontro.
Questo processo avviene anche nelle patologie autoimmuni.
La memoria immunologica si sviluppa prima dell’esordio del diabete e persiste per decenni, diventando quindi un problema nelle terapie di sostituzione delle beta cellule, inclusi trapianto di isole e di pancreas.
Cellula Staminale della Memoria
Tuttavia, il gruppo del Dr. Monti è riuscito a trovare il tallone d’Achille di queste cellule, che è rappresentato dalla loro dipendenza dal glucosio come carburante per produrre energia: bloccando il recettore che le cellule usano per approvvigionarsi di glucosio (GLUT1) si può impedire sia la loro formazione che l’attivazione di quelle già presenti.
Il prossimo passo sarà sicuramente lo sviluppo di un modello pre-clinico per testare l’efficacia di potenziali farmaci ed eventuali effetti avversi non rilevabili in vitro così da capire se è possibile e ragionevole trasferire questo approccio nell’uomo.
In attesa che questo approccio venga trasferito alla fase pre-clinica, si cerca di trovare siti nel corpo umano in cui le isole non vengano “viste” dal sistema immunitario.
In collaborazione con il prof. Piemonti, è stata quindi esplorata la possibilità di trapiantare le isole in un sito anatomico in cui il sistema immunitario sia meno attivo.
Un sito alternativo con queste caratteristiche è il midollo osseo che in modelli pre-clinici si è dimostrato essere inaccessibile al sistema immunitario. Purtroppo, nel lavoro presentato è stato mostrato come il midollo osseo umano sia però in grado di sviluppare una riposta immunitaria molto potente che causa la perdita delle isole trapiantate: il midollo non è quindi idoneo ad essere un sito “alternativo” al fegato per il trapianto di isole.
Diabete e iPSC: nuovi sviluppi tecnologi per il futuro della patologia.
La Beta Cell Biology Unit dell’istituto ha presentato invece i progressi del suo lavoro sulle cellule staminali pluripotenti indotte (iPSC), che sono cellule staminali capaci di differenziare in tutti i tipi cellulari proprio come le cellule staminali embrionali, pur originando da una cellula adulta.
In particolare la dott.ssa Silvia Pellegrini ha presentato i dati su una molecola che, aggiunta alle iPSC durante il differenziamento in beta cellule, ne aumenta l’efficienza agendo a livello epigenetico – cioè sulle proteine che interagiscono col DNA nel determinare il destino di una cellula. Il dott. Raniero Chimienti invece ha raccontato di come le iPSC siano state rese invisibili al sistema immune tramite un “taglia e cuci” genetico, mentre la dott.ssa Valeria Sordi ha descritto la generazione di iPSC da un paziente con diabete monogenico e la possibilità di ottenere beta cellule come modello di malattia.
L’Unità Beta Cell Biology del prof. Piemonti si occupa anche di sviluppare l’ambizioso progetto, finanziato dall’Ospedale San Raffaele e sviluppato in particolar modo dal dott.Citro, in cui viene proposta la combinazione di due diverse tecnologie implicate nella cura del diabete di tipo 1: la medicina rigenerativa e l’ingegneria tissutale, branche della scienza che attualmente corrono in parallelo, integrando e migliorando le soluzioni proposte dalla medicina tradizionale per la cura di numerose patologie.
In particolare, l’obiettivo principale del progetto è la rigenerazione in vitro della funzione endocrina del tessuto pancreatico attraverso: 1) la decellularizzazione d’organo e 2) l’impiego di cellule staminali iPSC terminalmente differenziate a cellula endoteliale (cellule che “formano” i vasi sanguigni) e a beta cellula. Decellularizzare significa privare un organo di qualsiasi cellula che lo compone mantenendo intatta la struttura originaria dell’organo in questione: la decellularizzazione d’organo afferisce alla branca dell’ingegneria tissutale e permette la creazione di “contenitori vuoti”. Le iPSC fanno invece parte della medicina rigenerativa e vengono ad oggi impiegate per la rigenerazione programmata di diversi gruppi cellulari. Combinando queste due tecnologie sarà possibile generare un organo vuoto che sarà ripopolato dalle iPSC terminalmente differenziate a beta cellule e a cellule endoteliali al fine di ristabilire la funzione pancreatica.
Il successo di questo studio potrebbe aprire nuove opportunità nella creazione di organi endocrini biocompatibili per la sostituzione beta cellulare nel diabete di tipo 1.
Le cellule T, causa di produzione di autoanticorpi e un aiuto per la tolleranza al trapianto.
Gli altri studi di ricerca presentati al retreat sono stati quelli riguardanti l’immunologia di base e traslazione studiata del gruppo della dott.ssa Georgia Fousteri: in particolar modo, gli studi si concentrano sullo studio delle popolazioni cellulari ritenute importanti per la perdita di tolleranza al trapianto di isole (cellule TR1) ma anche quelle responsabili alla regolamentazione degli auto-anticorpi (cellule TFH e TFR).
Le cellule follicolari helper (TFH) e regolatorie (TFR) sono una sottoclasse di cellule T – cellule immunitarie responsabili della protezione verso le infezioni – specializzate in modo esclusivo alla stimolazione e alla regolazione della produzione di anticorpi: una deregolazione del numero e della funzionalità delle TFH e TFR provoca la produzione di autoanticorpi, come quelli contro l’insulina.
Mentre le TFH stimolano la produzione di anticorpi, le TFR hanno il ruolo di inibire la produzione anticorpale e quindi controllare l’autoimmunità, proteggendo dalla comparsa di autoanticorpi diretti verso le isole pancreatiche.
Essendo gli autoanticorpi associati al riconoscimento delle isole pancreatiche, il gruppo ha ritenuto importante studiare il comportamento delle TFH e TFR.
Analizzando il sangue, i linfonodi pancreatici e la milza di pazienti pediatrici e adulti con T1D, si è osservato che la patogenesi nasce da un graduale disequilibrio tra le cellule di TFH e TFR, portando ad un declino delle funzionalità pancreatica: questo è ciò che permetterà di costruire le prime basi per una terapia volta a riportare equilibrio tra TFH e TFR.
Le cellule T regolatorie sono una sottoclasse di cellule T molto importante per il funzionamento dei meccanismi di difesa del nostro organismo: sono specializzate infatti nel mantenimento della “tolleranza immunologica”, ossia il meccanismo che permette al sistema immunitario di combattere i patogeni senza aggredire i tessuti dell’organismo. Esistono diversi tipi di cellule T regolatorie e tra queste quelle di tipo 1 (TR1) sono molto importanti nella prevenzione e nella cura di malattie autoimmuni come il diabete di tipo 1, ma anche nella soppressione del rigetto dopo il trapianto d’organo.
Utilizzando un modello murino di trapianto di isole pancreatiche, il gruppo della dott.ssa Fousteri ha osservato che la terapia cellulare con le TR1 ha promosso la tolleranza al trapianto e questa tolleranza è stata mantenuta anche in caso di infezione virale acuta: le cellule TR1 rappresentano quindi una possibile efficace terapia per promuovere la tolleranza e migliorare il rigetto del trapianto, dando così nuove speranze di cura per il futuro della patologia.


